Mecaneg cwantwm
 | |
| Enghraifft o'r canlynol | damcaniaeth, cangen o ffiseg |
|---|---|
| Math | mecaneg |
| Crëwr | Max Planck, Albert Einstein, Louis de Broglie, Erwin Schrödinger, Werner Heisenberg, John von Neumann, Paul Dirac, Wolfgang Pauli, Max Born, Pascual Jordan, John Stewart Bell |
| Rhan o | ffiseg fodern, quantum physics |
| Dyddiad cyhoeddi | 1900 |
| Mecaneg cwantwm | ||||||||||||||
| Werner Heisenberg a Erwin Schrödinger sefydlwyd mecaneg cwantwm | ||||||||||||||
Prif dudalen Ffiseg
| ||||||||||||||
Mecaneg cwantwm yw'r gangen o ffiseg sy'n delio ag ymddygiad mater ac egni ar raddfa fach iawn. Mae mecaneg cwantwm yn sylfaen i'n hymwybyddiaeth o pob grym sylfaenol natur gan eithrio disgyrchiant. Mae mecaneg cwantwm hefyd yn sylfaen i nifer o ganghenau o ffiseg gan gynnwys electromagnetedd, ffiseg gronnynau, ffiseg mater cyddwysedig a hyd yn oed rhannau o gosmoleg. Mae bondio cemegol, nanotechnoleg, trydaneḥg a thechnoleg gwybodaeth hefyd wedi'i selio ar fecaneg cwantwm. Mae yna ganrif o arbrofion wedi profi'n llwyddiannus.
Hanes[golygu | golygu cod]
Ar ddechrau'r ugeinfed ganrif roedd gwyddonwyr yn credu bod bron popeth sydd i'w ddarganfod wedi'i ddarganfod a taw dim ond mesuriadau gwell oedd ar ôl i'w gwneud. Fe gredid fod goleuni wedi'i wneud o donnau a bod mater wedi'i wneud o ronynnau ac y gellid eu disgrifio drwy ddeddfau clasurol. Fodd bynnag roedd mesuriadau newydd yn dangos priodweddau rhyfedd i oleuni a mater na ellid eu hesbonio. Yn 1900 fe ddangosodd Max Planck fod egni’r ymbelydredd electromagnetaidd a allyrir gan gyrff du yn gyfrannol ag amledd y don ac nid â’i thanbeidrwydd na’i hosgledd fel y rhagddywed mecaneg clasurol. Fe fformiwleiddiodd yr hafliad:
ble E yw’r egni, f yw’r amledd, a h yw cysonyn Planck gyda’r gwerth 6.626 x 10−34 Js.
Rhwng 1907 a 1917 roedd arbrofion a wnaethpwyd gan Ernest Rutherford yn dangos bod atomau wedi'u cyfansoddi o gnewyllyn dwys positif wedi'i amgylchynnu gan electronau bach negatif. Roedd y darganfyddiad hwn yn drychinebus gan fod mecaneg clasurol yn rhagddweud y byddai atom o'r fath yn ansefydlog; byddai'r electronau yn cyflymu tuag at y cnewyllyn dan yr atyniad electrostatig gan allyrru ymbelydredd electromagnetaidd a cholli egni nes i'r ddau ymasio.
Roedd arbrofion sbectrosgopaidd hefyd yn dangos priodweddau rhyfedd i atomau. Wrth gynhesu nwyon dan gerrynt maent yn dechrau tywynnu. Os mae'r goleuni a allyrrir yn cael ei ddiffreithio fe welir cyfres o linellau arwahanol ar donfeddi penodol sy'n nodweddiadol iawn o'r elfen.
Model Bohr[golygu | golygu cod]
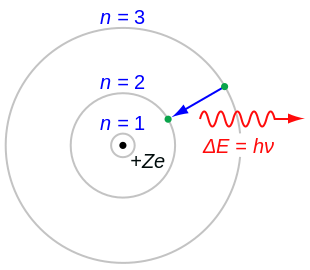
Fe esboniwyd hyn gan Niels Bohr a gyhoeddodd ei fodel o'r atom yn 1913. Fe ragdybiodd y canlynol:
- Mae electronau yn teithio mewn orbitau cylchol o amgylch y cnewyllyn.
- Pan fo’r electron mewn un o’r orbitau nid ydyw’n allyrru ymbelydredd.
- Gall electron neidio o un orbit i orbit egni uwch yn bellach o’r niwclews drwy amsugno ymbelydredd.
- Pan mae electron yn neidio yn ôl lawr i’r orbit egni is mae’n rhyddhau ymbelydredd. Mae egni’r ymbelydredd hwn yn hafal i’r gwahaniaeth egni rhwng y ddau orbit.
Roedd y syniad hwn o orbitau sefydlog yn seliedig ar y ffaith bod y llinellau sbectrosgopaidd yn arwahanedig. Pe allai’r electron fod mewn unrhyw orbit gydgag unrhyw egni byddai’r sbectrwm o donfeddi a allyrrir yn barhaol fel enfys. Felly fe gyflwynodd Bohr y rheol gwantwm bod momentwm onglog wedi ei gwanteiddio mewn unedau integrol o h/2π:
Fe ddefnyddiodd Bohr y rheol gwantwm hon i ddeillio mynegiad lefau egni yr atom hydrogen:
Nid esboniodd Bohr ddeilliad y cwanteiddiad hwn yn ei fodel ond ei lwyddiant oedd esbonio’r arsylwadau sbectrosgopaidd yn nhermau strwythur yr atom. Ac yn wir roedd ei fodel yn gweithio'n berffaith ar gyfer hydrogen.
Deuoliaeth gronyn-ton[golygu | golygu cod]
Pan mae ymbelydredd uwch-fioled yn cael ei ddisgleirio ar fetel mae electronau yn cael eu rhyddhau. O dan amledd penodol nid yw electronau yn cael ei ryddhau heb ots am danbeidrwydd y goleuni. Roedd hyn yn anghytuno gyda'r syniad a dderbyniasid am ganrifoedd bod goleuni wedi'i wneud o donau gan fod model o'r math yn rhagddweud y byddai unrhyw amledd yn arwain at allyriad electronau. Hynny yw yn ôl y tonfodel byddai'r electron yn "storio" egni o'r ton goleuni nes bod ei egni yn fwy nag egni ioneiddiad y metel.
Fe esboniwyd yr effaith ffotoelectrig gan Einstein a gynigodd bod goleuni wedi'i wneud o gronynnau a'u galwodd yn ffotonau. Yn seliedig ar waith Planck fe gynigodd bod egni ffoton yn gyfrannol ag amledd y don electromagnetaidd a gysylltir gyda'r ffoton, E = hf. Mae'n debygol bod un ffoton yn gwrthdaro gydag un electron ac os mae ei egni cinetig yn fwy nag egni ioneiddio'r atom, caiff yr electron ei allyrru.
Roedd gwaith Einstein yn ddechrau'r cysyniad o ddeuoliaeth gronyn-ton.
Egwyddor Ansicrwydd Heisenberg a Thonfecaneg Schrödinger[golygu | golygu cod]
Yn 1923 dangosodd Louis de Broglie bod gan bob gronyn cwantwm donfedd mewn perthynas isdro gyda'u fomentwm:
Yn seliedig ar y gwaith hwn, yn 1926 creodd Erwin Schrödinger don hafaliad i ddisgrifio tonnau de Broglie:
ble
- yw'r egni potensial,
- yw'r ton ffwythiant,
- yw'r ail ddifferiad mewn tri dimensiwn.
Heddiw fe wyddwn taw hwn yw hafaliad sylfaenol mecaneg cwantwm a ellir ei ddatrys ar gyfer unrhyw system i ganfod ei thon ffwythiant sy'n disgrifio popeth a ellir ei wybod amdani. Fodd bynnag pan gyhoeddodd Schrödinger ei hafaliad ni wyddai yn union sut i ddehongli'r ton ffwythiant ac roedd y cwestiwn o sut all rhywbeth fodoli fel ton a fel gronyn ar yr un pryd yn dal i fod yn broblem. Yn 1927 dangosodd Werner Heisenberg bod ansicrwydd cynhenid o fewn systemau cwantwm ac nad ellir gwybod yn fanwl gywir ddau ddarn o wybodaeth ynglŷn â system yn gydamserol. Fe fformiwleiddiwyd y canlyniadau yn hafaliad Egwyddor Ansicrwydd Heisenberg:

ble
- yw'r ansicrwydd mewn momentwm
- yw'r ansicrwydd mewn safle
Hynny yw po gywiraf y gwyddwn fomentwm gronyn y lleiaf cywir y gallwn ddarganfod ei safle, a chroesymgroes.
Er mwyn cysoni'r ansicrwydd hwn gyda hafliad Schrödinger cynigodd Max Born bod tanbeidrwydd y ton ffwythiant ar rwy bwynt yn gysylltiedig â thebygolrwydd darganfod y gronyn ar y pwynt hwnnw. Hynny yw, mae sgwâr y ton ffwythiant yn ffwythiant dwysedd tebygolrwydd ac yn wir dyma'r dehongliad a dderbynnir heddiw. Er enghraifft ar gyfer gronyn sy'n teithio mewn un dimensiwn, gellir cyfrifo tebyglorwydd darganfod y gronyn rhwng dau bwynt a a b fel a ganlyn:
Llwyddiant hafaliad Schrödinger yw bod y ton ffwythiannau yn disgrifio popeth a ellir ei wybod ynglŷn â'r system. Mae'n rhagddweud yr un lefelau egni ar gyfer atom hydrogen ag mae model Bohr ond mae'n esbonio pam mae atomau'n sefydlog; hynny yw pam nad yw'r electron yn "cwympo" i mewn i'r cnewyllyn dan yr atyniad electrostatig. Yn ogystal mae tonfecaneg Schrödinger yn esbonio pam mae egni wedi'i gwanteiddio. Ar y llaw arall mae model Bohr yn rhagdybio cwanteiddiad fel priodwedd o systemau cwantwm na ellir ei esbonio. Gweler y drafodaeth isod am fwy o wybodaeth.
Gweithredwyr[golygu | golygu cod]
Mewn mecaneg cwantwm fe gysylltir gweithredwr mathemategol Ĝ, gyda phob maint arsylwadwy, er enghraifft gweithredwr momentwm yn gysylltiedig â momentwm, gweithredwr egni yn gysylltiedig ag egni, ayyb. Mae'r gweithredwyr hyn y mewnbynnu ffwythiant eigen ac yn allbynnu gwerth eigen:
Y gweithredwr momentwm mewn un dimensiwn yw:
Y gweithredwr egni cinetig mewn tri dimensiwn yw:
Ynghyd a'r egni potensial mae'r gweithredwr egni cinetig yn ffurfio'r gweithredwr Hamiltonian sef y gweithredwr egni:
Mae egni system felly'n gwerth-eigen Hamiltonian y system honno:
Mae'r hafaliad uchod yn ffurf o hafaliad Schrödinger sy'n annibynnol o amser.
Systemau sylfaenol[golygu | golygu cod]
Gronyn mewn blwch[golygu | golygu cod]
Un o'r systemau symlaf y gellir canfod datrysiadau analytig ar ei chyfer yw'r gronyn mewn blwch. Yn y system hon, mae gronyn yn bodoli o fewn potensial ffynnon sgwâr un dimensiwn gyda'r hyd L. Hynny yw y tu mewn i'r blwch (0 < x < L) mae'r egni potensial, V(x), yn hafal i 0 ac ar y muriau (x = 0, L) mae'r egni potensial yn codi'n sydyn i anfeidredd. Yn glasurol gellir meddwl am y system hon fel gronyn yn teithio yn ôl ac ymlaen ac yn gwrthdaro gyda'r muriau heb golli egni na momentwm iddynt.
Datrysiad[golygu | golygu cod]

Gan fod yr egni potensial yn hafal i 0, mae ffurf hafaliad Schrödinger fel a ganlyn:
Gellir rhannu'r hafaliad differol rhannol hwn i mewn i ddau hafaliad differol cyffredin drwy dybio y gellir mynegi'r ton ffwythiant fel:
Mae hyn yn rhoi hafaliad sy'n dibynnu ar amser t:
ac yn fwy arwyddocaol hafaliad sy'n dibynnu ar safle x:
Yn y ddau hafaliad uchod, cysonyn E yw'r egni. Ar ôl datrys y ddau hafaliad a chyfuno'r ddau ddatrysiad ceir y ton ffwythiant:
Fodd bynnag, gan fod y gronyn yn wedi'i gyfyngu y tu mewn i'r blwch, ni all fodoli y tu allan i'r blwch ac felly mae'n rhaid bod osgledd y ton ffwythiant yn hafal i 0 ymhoban heblaw am rhwng x = 0 ac x = L. Felly mae'n rhaid i'r tonffwythiant fynd i 0 ar y muriau ac er mwyn sicrhau hyn fe osodwn ddau amod ffin:
Mae Asin(kx) = 0 pan mae x = 0 ac felly mae hyn ddatrysiad derbyniol. Ar y llaw arall mae Bcos(kx) = B pan mae x = 0 felly nid yw'r rhan hwn yn dderbyniol. Er mwyn boddhau yr ail amod ffin mae'n rhaid bod sin(kx) hafal i 0, ac mae hyn yn wir os:
- ble
Er y byddai n = 0 yn foddhaol yn fathemategol, nid ydyw'n dderbyniol yn ffisegol gan y byddai'r tonffwythiant yn hafal i 0 ymhobman a byddai'r ansicrwydd ym momentwm y gronyn yn union yn 0 sy'n torri'r egwyddor ansicrwydd. Felly y gyfres o donffwythiannau a gawn yw:
gydag egni sydd wedi ei gwanteiddio gan n:























![{\displaystyle \Psi (x,t)=[A\sin(kx)+B\cos(kx)]e^{-iwt}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/61bf96d4b2134a673e8f2358be2c3034524822b3)





